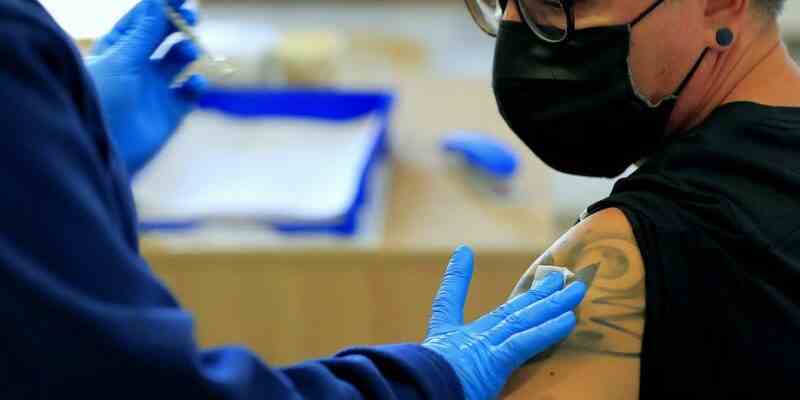
Laut Marco Cavaleri, Head of Vaccine Strategy der European Medical Authority (EMA), gibt es noch nicht genügend Beweise, um zusätzliche COVID-19-Booster zu rechtfertigen, während BioNTech Pfizer bereits eine Zulassung für zusätzliche Impfungen in den USA beantragt hat
Europa hat eine hohe Impfrate, wobei über 70 % der Europäer die Grundimmunisierung abschließen und die Hälfte eine Auffrischimpfung erhält. Aber wenn es um zusätzliche Auffrischungsdosen geht, hat die EMA hielt an seiner Stellungnahme vom Januar fest.
„Sie haben Erklärungen einiger Impfstoffentwickler gesehen, die die Notwendigkeit einer zweiten Auffrischimpfung betonen. Ich möchte noch einmal betonen, dass es aus regulatorischer Sicht noch nicht genügend Beweise gibt, weder aus klinischen Studien noch aus der Praxis, die unsere Empfehlung zur Notwendigkeit einer zweiten Auffrischungsimpfung in der Allgemeinbevölkerung stützen“, sagte er Cavaleri, Head of Biological Health Threats and Vaccines Strategy bei der EMA, zur Pressekonferenz am Donnerstag (17. März).
Da Israel bei den Impfraten führend ist und Ende Dezember 2021 als erstes Land mit der Verabreichung zweiter Auffrischungsdosen begann, beobachten alle Arzneimittelbehörden und Wissenschaftler die Entwicklungen.
Israelische Daten zeigen eine zweite Auffrischimpfung bei medizinischem Personal wurden die Antikörperspiegel wieder auf die Werte nach der ersten Auffrischungsimpfung zurückgesetzt, sagte Cavaleri.
„Wir sehen keinen wirklichen Anstieg, aber wir sehen eine Wiederherstellung des Antikörperspiegels“, sagte er und fügte hinzu, dass „die Infektionsprävention eher begrenzt war“. Aus diesem Grund betonte Cavaleri, dass es mFür junge Erwachsene sei es möglicherweise nicht „ein großer Vorteil, zu diesem Zeitpunkt eine zweite Auffrischungsimpfung zu verabreichen“.
Vierter Schuss für ältere und immunsupprimierte Personen
Anders sieht es bei älteren und immunsupprimierten Menschen aus. Eine weitere Studie aus Israel zeigte, dass die zweite Auffrischimpfung, die mindestens bis zu fünf Monate nach der ersten Auffrischimpfung verabreicht wurde, bei einer älteren Bevölkerung Krankenhausaufenthalte reduzierte, sagte Cavaleri.
„Es wird wichtig sein, mehr Beweise zu sammeln, um ein klareres Bild davon zu bekommen, welchen Wert die Verabreichung einer zweiten Auffrischimpfung mit der aktuellen Impfstoffzusammensetzung hat und was der beste Zeitpunkt sein könnte“, fügte er hinzu.
Aber während die EMA Beweise sammelt, haben einige EU-Länder bereits zweite Auffrischungsimpfungen eingeführt. Am 3. März, Das kündigte Cavaleri an Einige Mitgliedstaaten hatten damit begonnen, älteren Menschen über 70 oder 80 Jahren eine zweite Auffrischimpfung zu verabreichen.
„Dieser Ansatz wird durch die Tatsache gerechtfertigt, dass ältere Menschen in Bezug auf die Erlangung einer Immunität und das Risiko eines schweren COVID anfälliger wären als jüngere Erwachsene“, sagte er.
Zweite Auffrischungsdosen werden bereits in Italien eingeführt, wo zusätzliche Auffrischungsimpfungen für immunsupprimierte Personen verfügbar sind. In Ungarn die vierte Spritze für alle, die eine ärztliche Empfehlung haben, Radiofreies Europa Berichte.
In der Zwischenzeit haben Impfstoffentwickler, Deutschlands BioNTech und der US-Pharmariese Pfizersind zuversichtlich, dass die zusätzliche vierte Dosis ihres Impfstoffs benötigt wird.
BioNTech/Pfizer überzeugt, dass ein zweiter Booster benötigt wird
Am Dienstag (15. März) beantragte BioNTech Pfizer bei der US-amerikanischen Food and Drug Administration (FDA) die Zulassung einer zusätzlichen Auffrischimpfung für Erwachsene ab 65 Jahren, die eine erste Auffrischimpfung mit einem der zugelassenen oder zugelassenen COVID erhalten haben -19 Impfstoffe, heißt es in der Pressemitteilung von Pfizer.
Die Anwendung basiert auf Daten aus Israel. „Die Daten zeigten Hinweise darauf, dass ein zusätzlicher mRNA-Booster die Immunogenität erhöht und die Raten bestätigter Infektionen und schwerer Erkrankungen senkt“, heißt es in der Erklärung weiter.
Aufzeichnungen des israelischen Gesundheitsministeriums zeigten, dass die COVID-Raten bei 1,1 Millionen Erwachsenen ab 60 Jahren, die eine zusätzliche Auffrischungsdosis des Pfizer-BioNTech-Impfstoffs erhielten, doppelt so niedrig und die Rate schwerer Erkrankungen viermal niedriger waren als bei denen, die nur eine erhielten zusätzliche Dosis.
In der Pressemitteilung heißt es: „Eine zusätzliche Auffrischungsdosis des Pfizer-BioNTech-Impfstoffs, die mindestens vier Monate nach einer ersten Auffrischungsdosis verabreicht wird, könnte die Antikörpertiter auf die Spitzentiter nach der dritten Dosis wiederherstellen und den Schutz sowohl vor Infektionen als auch vor schweren Erkrankungen bei Personen verbessern 60 Jahren und älter in Israel und haben ein ähnliches Sicherheitsprofil wie frühere Dosen“.
Bisher habe die EMA keinen Antrag auf eine zweite Auffrischimpfung erhalten, sagte Cavaleri.
[Edited by Alice Taylor]