Der CEO von Pfizer sagt, das Unternehmen plane, die US-amerikanische Food and Drug Administration (FDA) „in Tagen“ um die Zulassung seines COVID-19-Impfstoffs bei jüngeren Kindern zu bitten.
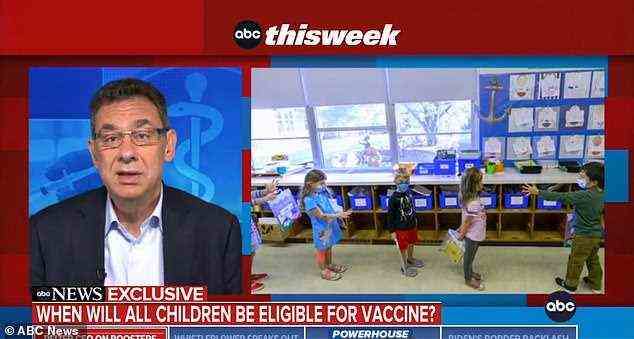
Am Sonntag wurde Albert Bourla in einem Auftritt bei ABCs This Week gefragt, wann das Land damit rechnen sollte, dass die Aufnahmen bei Kindern zwischen fünf und 11 Jahren genehmigt werden.
Das in New York ansässige Unternehmen hat zusammen mit seinem deutschen Partner BioNTech kürzlich Daten veröffentlicht, die belegen, dass der Impfstoff in geringeren Dosen bei Grundschulkindern sicher und wirksam ist.
“Ich denke, wir werden diese Daten ziemlich bald einreichen”, sagte Bourla gegenüber Gastgeber George Stephanopoulos.
“Es ist eine Frage von Tagen, nicht von Wochen, und dann liegt es an der FDA, die Daten zu überprüfen und zu ihren Schlussfolgerungen zu kommen und sie zu genehmigen oder nicht.”
Albert Bourla, CEO von Pfizer Inc, sagte am Sonntag gegenüber ABC This Week (oben), dass das Unternehmen seinen Antrag auf FDA-Zulassung seines Covid-Impfstoffs bei Kindern im Alter von 5 bis 11 Jahren „in Tagen“ einreichen werde.
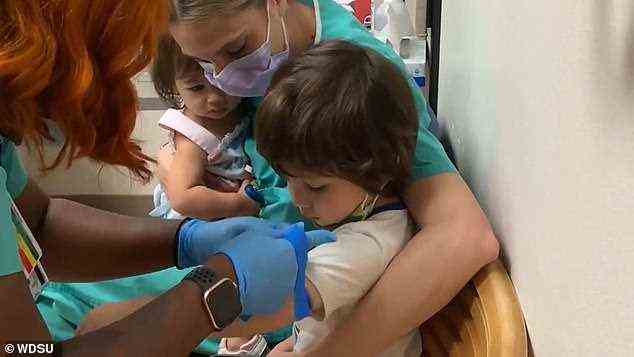
Kürzlich veröffentlichte Daten zeigten, dass der Impfstoff laut Pfizer bei jüngeren Kindern eine „robuste“ Immunantwort auslöste. Im Bild: Dr. Erin Biro hält ihren Sohn, als er in Pfizers klinischer Studie an jüngeren Kindern eine Spritze erhält
Laut Clinicaltrials.gov funktionierte Pfizers Studie bei jüngeren Kindern ähnlich wie bei älteren Kindern und Erwachsenen.
Insgesamt 4.500 jüngere Kinder im Alter von sechs Monaten bis 11 Jahren wurden an fast 100 klinischen Studienzentren in 26 US-Bundesstaaten, Finnland, Polen und Spanien eingeschrieben
Etwa die Hälfte der Gruppe im Alter von fünf bis 11 Jahren erhielt zwei Dosen im Abstand von 21 Tagen und die andere Hälfte erhielt Placebo-Spritzen.
Das Team testete dann die Sicherheit, Verträglichkeit und Immunantwort des Impfstoffs, indem es die Antikörperspiegel bei den jungen Probanden maß.
Pfizer sagte, es habe niedrigere Dosen für COVID-19-Impfstoffstudien bei Kindern ausgewählt als Teenager und Erwachsene.
Personen ab 12 Jahren erhalten zwei Dosen von 30 Mikrogramm (μg) des Impfstoffs.
Kinder im Alter zwischen fünf und 11 Jahren erhielten jedoch 10 μg-Dosen und Kinder im Alter von sechs Monaten bis vier Jahren erhielten drei μg-Dosen.
Bourla versicherte, dass Pfizer bereit wäre, diese kleineren Dosen im ganzen Land zu versenden, wenn die FDA die Injektion bei jüngeren Kindern genehmigt.
“Wenn sie es genehmigen, werden wir mit unserer Herstellung bereit sein, diese neue Formulierung des Impfstoffs bereitzustellen”, sagte er Diese Woche.
„Weil der Impfstoff, den die Kinder erhalten werden, eine andere Formulierung hat. Es ist ein Drittel der Dosis, die wir dem Rest der Bevölkerung geben.’
Im Gegensatz zu der größeren klinischen Studie, die an Erwachsenen durchgeführt wurde, wurde in der pädiatrischen Studie die Wirksamkeit nicht gemessen, indem die Zahl der COVID-19-Fälle in der Impfstoffgruppe mit der Zahl in der Placebo-Gruppe verglichen wurde.
Stattdessen untersuchten die Wissenschaftler die Konzentrationen neutralisierender Antikörper bei jungen Impfstoffempfängern und verglichen die Werte mit denen bei Erwachsenen.
Bis Ende des Jahres erwarten die Unternehmen Daten darüber, wie gut der Impfstoff bei Kindern zwischen zwei und fünf Jahren sowie zwischen sechs Monaten und zwei Jahren wirkt.
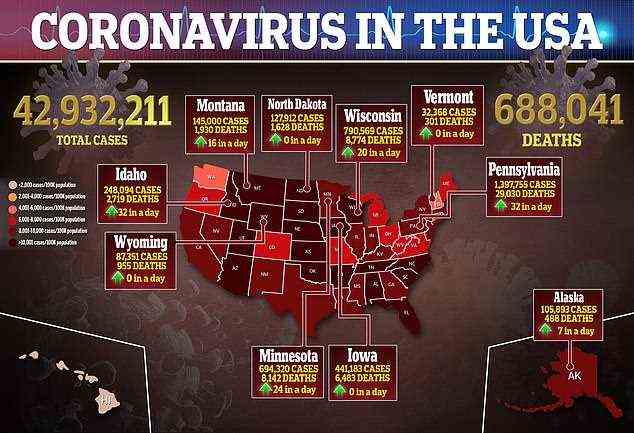
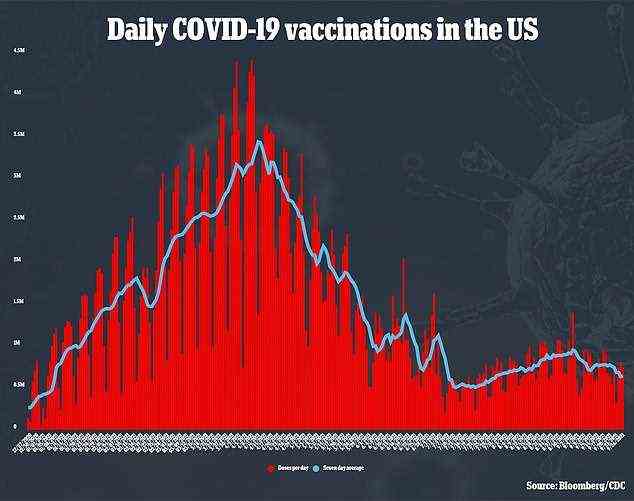
Vor kurzem stiegen auch die pädiatrischen Fälle von 71.726 pro Woche Anfang August auf mehr als 243.000 Anfang dieses Monats, angetrieben durch die Delta-Variante.
Laut der American Academy of Pediatrics scheinen sie jedoch jetzt mit 225.000 Meldungen in der vergangenen Woche rückläufig zu sein.
Außerdem gab es seit Beginn der Pandemie 480 Todesfälle bei Kindern, was darauf hindeutet, dass Kinder weniger als 0,1 Prozent aller Todesfälle ausmachen.
Derzeit gibt es keine Hinweise darauf, dass die Delta-Variante bei Kindern gefährlicher ist als frühere Virusstämme.
Aufgrund dieses geringen Risikos für schwere Erkrankungen haben Umfragen ergeben, dass viele Eltern ihre Kinder nicht impfen lassen.
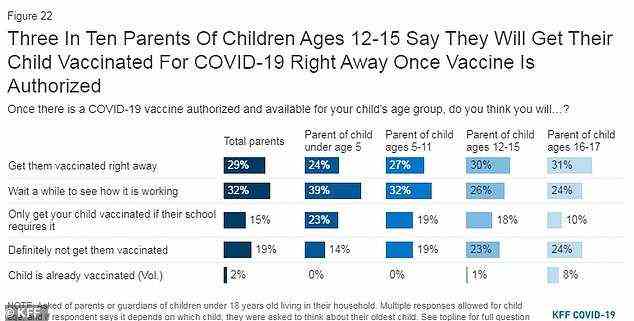
Einer Umfrage der Kaiser Family Foundation zufolge gaben 19% der Eltern von Kindern im Alter von fünf bis 11 Jahren an, ihre Kinder nur dann impfen zu lassen, wenn ihre Schule dies erfordert, und weitere 19% sagten, ihr Kind werde definitiv nicht geimpft werden
In einer von der Kaiser Family Foundation durchgeführten Umfrage im April 2021 wurden Eltern gefragt, ob sie ihr Kind impfen lassen würden, sobald ein COVID-19-Impfstoff zugelassen und für die Altersgruppe ihres Kindes verfügbar ist.
Von den Eltern zwischen fünf und elf Jahren sagten 27 Prozent, dass sie ihr Kind „sofort“ impfen lassen würden, und 32 Prozent sagten, sie würden abwarten, wie es funktioniert.
Neunzehn Prozent gaben an, ihre Kinder nur dann impfen zu lassen, wenn es die Schule erfordert, und weitere 19 Prozent sagten, ihr Kind werde definitiv nicht geimpft werden.
Eine Umfrage vom Juli 2021, die von der CS Mott Children’s Hospital National Poll on Children’s Health in Michigan Medicine durchgeführt wurde, ergab ähnliche Ergebnisse.
Von den Eltern von Kindern im Alter von drei bis 11 Jahren gaben 49 Prozent an, dass ihre Kinder wahrscheinlich einen Impfstoff erhalten würden, und 51 Prozent hielten dies für unwahrscheinlich.