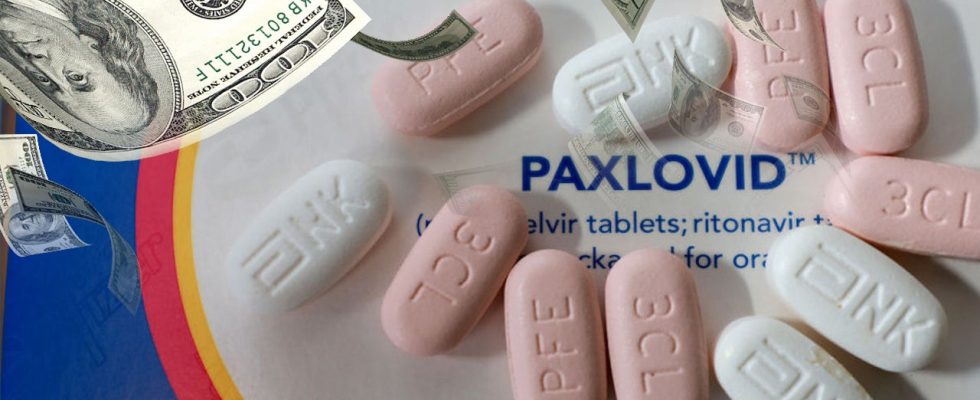
Paxlovid, eine antivirale Therapie, die verschrieben wird COVID-19-Patienten um schweren Erkrankungen vorzubeugen, wird die Anschaffung bald deutlich teurer.
Während das Medikament auf den kommerziellen Markt gelangt, hat Pfizer den aktualisierten Preis für eine fünftägige Kur auf 1.390 US-Dollar festgelegt – mehr als das Doppelte der 529 US-Dollar, die die Bundesregierung für die Behandlung gezahlt hatte.
Die neuen Preise wurden in einem Brief bekannt gegeben, den Pfizer am 18. Oktober an die Apotheken schickte und der dem Wall Street Journal vorliegt.
COVID-19-Erholung nach der Behandlung mit Paxlovid, wahrscheinlich aufgrund unzureichender Exposition gegenüber dem Medikament
„Die Preisgestaltung für Paxlovid basiert auf dem Wert, den es Patienten, Anbietern und Gesundheitssystemen bietet, da es eine wichtige Rolle bei der Reduzierung von Krankenhausaufenthalten und Todesfällen im Zusammenhang mit COVID-19 spielt“, sagte Pfizer in einer Erklärung.
Letzte Woche gab Pfizer in einer Pressemitteilung auf seiner Website bekannt, dass es „seinen Liefervertrag mit der US-Regierung für Paxlovid geändert hat“, da die mit der Notfallzulassung (EUA) gekennzeichneten Medikamente auslaufen.
Paxlovid, eine antivirale Therapie, die COVID-19-Patienten zur Vorbeugung schwerer Erkrankungen verschrieben wird, wird bald deutlich teurer in der Anschaffung sein. (Getty Images)
Der Übergang von Paxlovid zum kommerziellen Markt – und zu seinem aktualisierten Preismodell – soll im November dieses Jahres beginnen.
„Der kommerzielle Übergang wird im November 2023 beginnen, wenn die US-Regierung damit beginnt, den Vertrieb von Paxlovid mit EUA-Kennzeichnung einzustellen“, schrieb Pfizer.
AKTUALISIERTE COVID-IMPFSTOFFE: FDA KÜNDIGT NOTFALLZULASSUNG UND AUTORISIERUNG AN
Das Unternehmen wies darauf hin, dass der Listenpreis des Medikaments nicht unbedingt dem entspreche, was die Patienten aus eigener Tasche bezahlen würden.
„Pfizers Ziel ist es wie immer, einen breiten und gleichberechtigten Zugang zu unseren Medikamenten zu gewährleisten“, schrieb das Unternehmen in dem Brief.
„Wir arbeiten intensiv mit den Kostenträgern zusammen, um die bestmögliche Formulierungsplatzierung für Paxlovid zu erreichen, was zu niedrigen Eigenkosten (OOP) für die Patienten führt.“

Pfizer gab letzte Woche in einer Pressemitteilung auf seiner Website bekannt, dass es „seinen Liefervertrag mit der US-Regierung für Paxlovid geändert“ habe, da die mit der Notfallzulassung (EUA) gekennzeichneten Medikamente auslaufen. (iStock)
Pfizer sagte, es plane auch, ein Zuzahlungsprogramm für „berechtigte privat versicherte Patienten“ anzubieten, die das Medikament möglicherweise kostenlos erhalten könnten.
In seiner eigenen Pressemitteilung verwies Pfizer auch auf ein Patientenhilfsprogramm (PAP), bei dem Patienten, die Medicare und Medicaid beziehen – sowie diejenigen, die nicht versichert sind – Paxlovid bis 2024 kostenlos erhalten.
KLICKEN SIE HIER, UM UNSEREN GESUNDHEITS-NEWSLETTER ZU ANMELDEN
Paxlovid ist eine Kombination aus zwei antivirale MedikamenteNirmatrelvir und Ritonavir.
Patienten mit leichten bis mittelschweren Fällen von COVID nehmen während der fünftägigen Behandlung zwei Dosen jedes Arzneimittels ein.
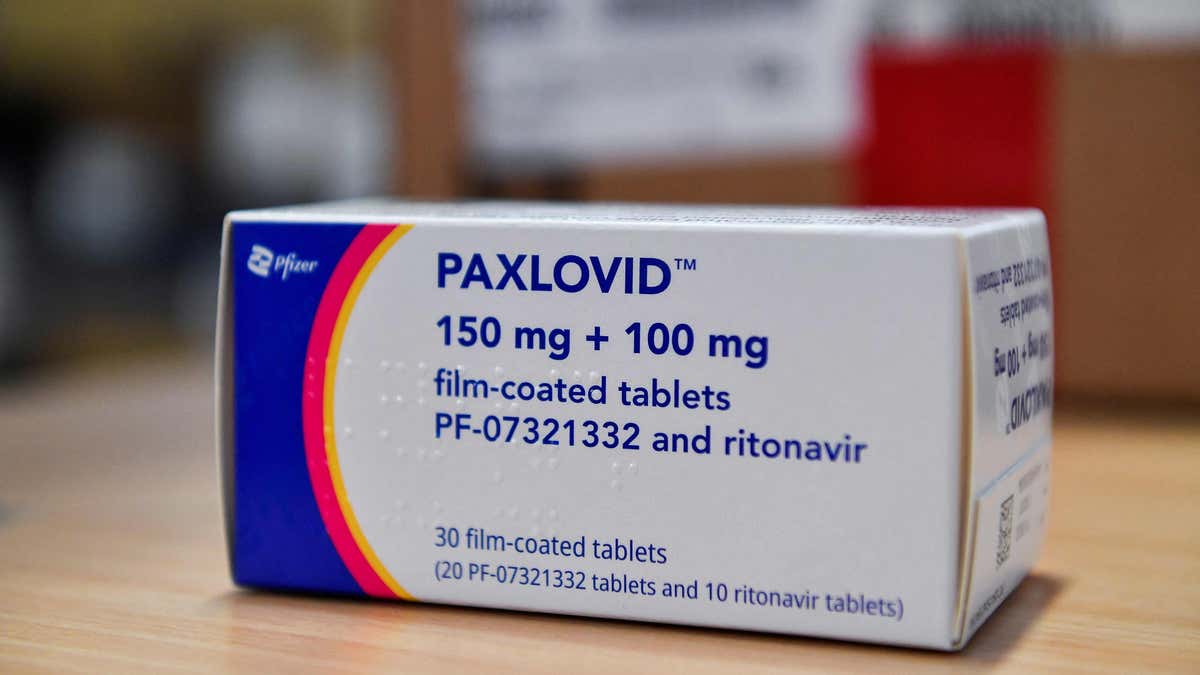
„Der kommerzielle Übergang wird im November 2023 beginnen, wenn die US-Regierung damit beginnt, den Vertrieb von Paxlovid mit EUA-Kennzeichnung einzustellen“, schrieb Pfizer. (REUTERS/Jennifer Lorenzini/File Photo)
In einer Erklärung des US-Gesundheitsministeriums (HHS) wurde auch die bevorstehende Umstellung von Paxlovid angekündigt.
„HHS wird in den nächsten Monaten einen reibungslosen und vorhersehbaren Übergang zum kommerziellen Markt gewährleisten und gleichzeitig unsere von HHS beschafften Behandlungskurse für Menschen mit Medicare und Medicaid sowie für diejenigen, die nicht versichert sind, priorisieren und reservieren“, schrieb das HHS in der Pressemitteilung.
KLICKEN SIE HIER, UM DIE FOX NEWS-APP ZU ERHALTEN
Das Datum 11. Mai 2023 markierte das offizielle Ende des bundesstaatlichen Gesundheitsnotstands im Zusammenhang mit der COVID-19-Pandemie.
In der Erklärung der Regierung wurde jedoch darauf hingewiesen, dass Notfallgenehmigungen für COVID-bezogene Produkte nicht betroffen seien.
„Der Zeitpunkt für den Abschluss der EUA muss noch festgelegt werden; sie wird nicht wie die anderen Erklärungen am 11. Mai 2023 abgeschlossen sein.“
Fox News Digital hat Pfizer um einen weiteren Kommentar gebeten.
Weitere Gesundheitsartikel finden Sie unter www.foxnews.com/health.