Im Kampf um die Verringerung der Menge gefährlicher, vom Menschen verursachter Chemikalien für die Ewigkeit in der Umwelt wurde ein Durchbruch erzielt.
Perfluoralkyl- und Polyfluoralkylsubstanzen (PFAS) werden in der Gesellschaft vielfältig verwendet, wurden aber auch mit Krebs und anderen Gesundheitsproblemen in Verbindung gebracht.
Sie sind dafür bekannt, dass sie extrem allgegenwärtig sind, wobei eine kürzlich durchgeführte Studie behauptet, dass Regenwasser überall auf der Erde gefährliche Werte aufweist.
Dies liegt teilweise daran, dass der Abbau von PFAS Tausende von Jahren dauern kann, aber Wissenschaftler der University of California, Los Angeles (UCLA) und der Northwestern University haben einen neuen Weg entdeckt, sie abzubauen.
Sie initiierten eine chemische Reaktion, die an zehn verschiedenen PFAS „wegknabberte“, indem sie kontaminiertes Wasser mit kostengünstigen Reagenzien erhitzten.
Die Technologie, die zu keinen schädlichen Nebenprodukten führte, könnte es Wasseraufbereitungsanlagen letztendlich erleichtern, die Chemikalien aus dem Trinkwasser zu entfernen.
Es gibt etwa 12.000 PFAS, die vielfältig eingesetzt werden können, unter anderem in Brandbekämpfungsschäumen, Antihaftbeschichtungen auf Bratpfannen und Textilien. Es wird angenommen, dass sie durch Industrieemissionen, Übertragung aus Verpackungen, Abwasser und Verdunstung aus den Schäumen in den Wasserkreislauf gelangen (Archivbild)

Die Langlebigkeit von PFAS ist einer Bindung zu verdanken, die sie alle zwischen Kohlenstoff- und Fluoratomen enthalten, die nichts in der Natur brechen kann
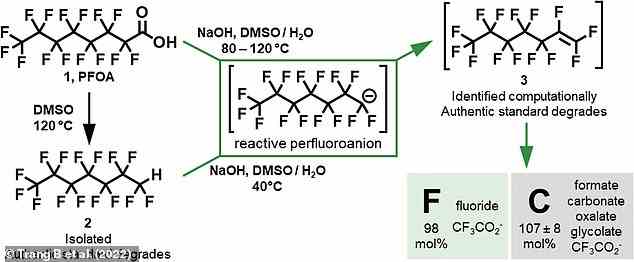
PFCA-Moleküle (oben links) bestehen aus einer langen Kohlenstoffkette mit daran gebundenen Fluoratomen, haben aber an einem Ende auch zwei negativ geladene Sauerstoffatome. Diese ist als „Carbonsäuregruppe“ bekannt und kann mit anderen Molekülen reagieren. Nach dem Erhitzen des PFCA in Wasser mit Dimethylsulfoxid (DMSO) und Natronlauge wird diese Carbonsäuregruppe abgespalten und bildet Wasser (Mitte). Dies löste dann eine chemische Reaktion aus, die „allmählich an dem Molekül herumknabberte“, so der Mitautor und UCLA-Professor Kendall Houk. Im Bild: Übersicht über die Abbauwege während der Reaktion
Es gibt etwa 12.000 PFAS, die vielfältig eingesetzt werden können, unter anderem in Brandbekämpfungsschäumen, Antihaftbeschichtungen auf Bratpfannen und Textilien.
Sie wurden erstmals in den 1940er Jahren entwickelt, aber seitdem haben viele wissenschaftliche Tests die synthetischen Chemikalien mit Gesundheitsproblemen in Verbindung gebracht.
Obwohl viele Hersteller sie aus ihren Produkten entfernen, werden sie immer noch routinemäßig überall um uns herum erkannt.
Ihre Langlebigkeit verdanken sie einer Bindung, die sie alle zwischen Kohlenstoff- und Fluoratomen enthalten, die nichts in der Natur brechen kann.
Es wird angenommen, dass PFAS durch Industrieemissionen, Übertragung aus Verpackungen, Abwasser und Verdunstung aus den Schäumen in die Umwelt gelangen.
Durch die extra starke Kohlenstoff-Fluor-Bindung passieren sie die meisten Wasseraufbereitungssysteme völlig unbeschadet.
Aus diesem Grund haben Wissenschaftler dringend versucht, Wege zu finden, um PFAS schnell aus kontaminierten Wasserquellen zu entfernen.
Die meisten aktuellen Technologien sind jedoch aggressiv und teuer und erfordern extrem hohe Temperaturen, spezielle Chemikalien oder Bestrahlung mit ultraviolettem Licht.
Einige der Techniken erzeugen Nebenprodukte, die ebenfalls schädlich sind und zusätzliche Schritte zur Entfernung erfordern.

PFAS oder Per- und Polyfluoralkylsubstanzen wurden erstmals in den 1940er Jahren entwickelt und sind heute in einer Vielzahl von Produkten zu finden, darunter Antihaftpfannen, wasserfeste Textilien und Brandschutzschäume
Die neue Methode, die heute in Science veröffentlicht wurde, erfordert nur übliche Laborreagenzien und Temperaturen zwischen 176 °F und 248 °F (80 °C und 120 °C).
Die Forscher konzentrierten sich auf Perfluoralkylcarbonsäuren (PFCAs), eine Art von PFAS, die zur Herstellung von Teflon verwendet wird.
Diese bestehen aus einer langen Kohlenstoffkette mit daran gebundenen Fluoratomen, haben aber an einem Ende auch zwei negativ geladene Sauerstoffatome.
Diese ist als „Carbonsäuregruppe“ bekannt und kann mit anderen Molekülen reagieren.
Nach dem Erhitzen des PFCA-Moleküls in Wasser mit Dimethylsulfoxid (DMSO) und Natronlauge wird diese Carbonsäuregruppe abgespalten und bildet Wasser.
Dies löste dann eine chemische Reaktion aus, die „allmählich an dem Molekül herumknabberte“, so der Mitautor und UCLA-Professor Kendall Houk.
Professor William Dichtel von der Northwestern University sagte: „Das löste all diese Reaktionen aus und fing an, Fluoratome aus diesen Verbindungen auszuspucken, um Fluorid zu bilden, das die sicherste Form von Fluor ist.
“Obwohl Kohlenstoff-Fluor-Bindungen superstark sind, ist diese geladene Kopfgruppe die Achillesferse.”
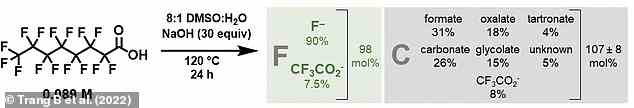
Was von der Reaktion zurückbleibt, ist eine Mischung aus harmlosen, natürlich vorkommenden kohlenstoff- und sauerstoffhaltigen Nebenprodukten
Wie experimentell und durch Computermodelle bestätigt wurde, waren die einzigen Nebenprodukte Kohlendioxid, Ameisensäure und Fluorid.
All dies ist nicht schädlich, letzteres wird oft Zahnpasta zugesetzt, um Karies vorzubeugen, was bedeutet, dass es keine Begrenzung gibt, wie viel Wasser auf einmal dekontaminiert werden kann.
Die Methode hat 10 Arten von PFCA erfolgreich abgebaut und ist gilt vermutlich für die meisten der 40 Prozent der PFAS, die Carbonsäuregruppen enthalten.
Die Forscher hoffen, dass dies auch zur Entdeckung von Technologien führen wird, die Tausende anderer Chemikalien ausrotten werden.
“Es gibt andere Klassen, die nicht die gleiche Achillesferse haben, aber jede wird ihre eigene Schwäche haben”, sagte Professor Dichtel in einer Erklärung.
“Wenn wir es identifizieren können, wissen wir, wie wir es aktivieren können, um es zu zerstören.”

