Forscher haben den ersten umfassenden Zellatlas eines Säugetiergehirns erstellt und über 32 Millionen Zellen im Mausgehirn kartiert. Dieser Atlas, Teil der NIH BRAIN Initiative, bietet beispiellose Einblicke in Gehirnzelltypen und -verbindungen, erweitert unser Verständnis des menschlichen Gehirns und hilft bei der Entwicklung neuer Behandlungsmethoden für Hirnerkrankungen. Bildnachweis: SciTechDaily.com
Ein bahnbrechender Zellatlas, der das gesamte Gehirn von Mäusen kartiert und über 32 Millionen Zellen detailliert darstellt, ebnet den Weg für ein tieferes Verständnis des menschlichen Gehirns und die Entwicklung präziser Therapien für Hirnerkrankungen.
Zum ersten Mal überhaupt hat ein internationales Forscherteam einen vollständigen Zellatlas eines gesamten Säugetiergehirns erstellt. Dieser Atlas dient als Karte für das Gehirn der Maus, beschreibt Typ, Lage und molekulare Informationen von mehr als 32 Millionen Zellen und liefert Informationen über die Konnektivität zwischen diesen Zellen. Die Maus ist das am häufigsten verwendete Wirbeltier-Versuchsmodell in der neurowissenschaftlichen Forschung, und diese Zellkarte ebnet den Weg für ein besseres Verständnis des menschlichen Gehirns – des wohl leistungsstärksten Computers der Welt. Der Zellatlas legt auch den Grundstein für die Entwicklung einer neuen Generation von Präzisionstherapeutika für Menschen mit psychischen und neurologischen Erkrankungen des Gehirns.
Die Ergebnisse wurden von den National Institutes of Health finanziert Hirnforschung durch die Weiterentwicklung innovativer Neurotechnologien® Initiative oder The BRAIN Initiative® und erscheinen in einer Sammlung von 10 Artikeln, die in veröffentlicht wurden Natur.
„Der Mausatlas hat das komplexe Netzwerk der Gehirnzellen von Säugetieren in einen beispiellosen Fokus gerückt und Forschern die Details geliefert, die sie zum Verständnis der menschlichen Gehirnfunktionen und -krankheiten benötigen“, sagte Joshua A. Gordon, MD, Ph.D., Direktor des National Institute of Psychische Gesundheit, Teil der Nationales Gesundheitsinstitut.
Detaillierte Kartierung des Mausgehirns
Der Zellatlas beschreibt die Zelltypen in jeder Region des Mausgehirns und ihre Organisation innerhalb dieser Regionen. Zusätzlich zu diesen Strukturinformationen bietet der Zellatlas einen unglaublich detaillierten Katalog des Transkriptoms der Zelle – den vollständigen Satz von Gen-Auslesungen in einer Zelle, der Anweisungen zur Herstellung von Proteinen und anderen Zellprodukten enthält. Die im Atlas enthaltenen transkriptomischen Informationen sind hierarchisch organisiert und beschreiben Zellklassen, Unterklassen und Tausende einzelner Zellcluster im Gehirn.
Der Atlas charakterisiert auch das Zellepigenom – chemische Modifikationen einer Zelle DNA und Chromosomen, die die Art und Weise verändern, wie die genetische Information der Zelle ausgedrückt wird – und beschreiben Tausende epigenomischer Zelltypen und Millionen möglicher genetischer Regulationselemente für verschiedene Gehirnzelltypen.
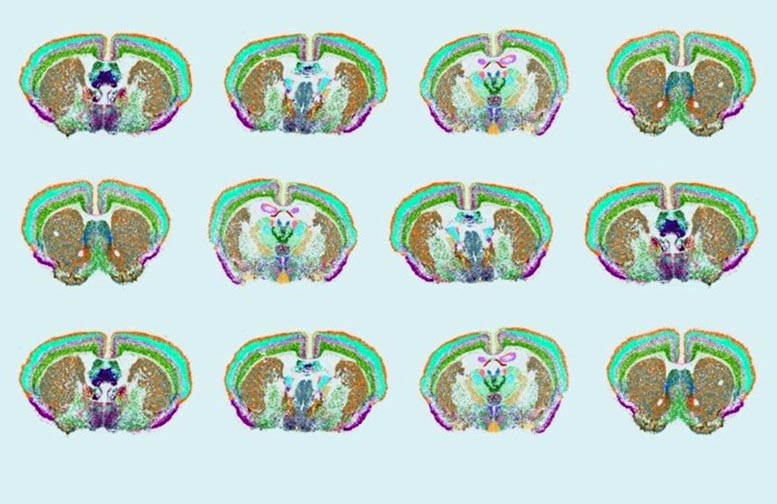
Räumliche Verteilung verschiedener Zelltypen im Gehirn der Maus. Hier wurde MERFISH verwendet, um 500 Gene im Gehirn von Mäusen zu messen, um die komplexe Verteilung der Zelltypen im gesamten Gehirn aufzudecken. Bildnachweis: Yao/van Velthoven/Zeng, Allen Institute
Zusammengenommen liefern die in diesem Atlas enthaltenen strukturellen, transkriptomischen und epigenetischen Informationen eine beispiellose Karte der zellulären Organisation und Diversität im Mausgehirn. Der Atlas bietet auch einen Überblick über die Neurotransmitter und Neuropeptide, die von verschiedenen Zellen verwendet werden, sowie über die Beziehung zwischen den Zelltypen im Gehirn. Diese Informationen können als detaillierte Blaupause dafür verwendet werden, wie chemische Signale in verschiedenen Teilen des Gehirns ausgelöst und übertragen werden. Diese elektrischen Signale sind die Grundlage dafür, wie Gehirnschaltkreise funktionieren und wie das Gehirn insgesamt funktioniert.
Wegweisende Zusammenarbeit und zukünftige Richtungen
„Dieses Produkt ist ein Beweis für die Leistungsfähigkeit dieser beispiellosen, bereichsübergreifenden Zusammenarbeit und ebnet unseren Weg für präzisere Gehirnbehandlungen“, sagte John Ngai, Ph.D., Direktor der NIH BRAIN Initiative.“
Von den 10 in dieser Sammlung enthaltenen Studien werden sieben durch das NIH BRAIN Initiative Cell Census Network (BICCN) und zwei durch die größere NIH BRAIN Initiative finanziert. Das Hauptziel des BICCN, einer bahnbrechenden, gemeinschaftlichen Initiative zum Verständnis des zellulären Aufbaus des Gehirns, besteht darin, eine umfassende Bestandsaufnahme der Zellen im Gehirn zu erstellen – wo sie sich befinden, wie sie sich entwickeln, wie sie zusammenarbeiten und wie sie funktionieren regulieren ihre Aktivität – um besser zu verstehen, wie sich Hirnstörungen entwickeln, fortschreiten und am besten behandelt werden.
„Durch die Nutzung der einzigartigen Natur seiner multidisziplinären und internationalen Zusammenarbeit konnte das BICCN erreichen, was keinem anderen Wissenschaftlerteam zuvor gelungen ist“, sagte Dr. Ngai. „Jetzt sind wir bereit für den nächsten großen Schritt – die Vervollständigung der Zellkarten des menschlichen Gehirns und des Gehirns nichtmenschlicher Primaten.“
Das BRAIN Initiative Cell Atlas Network (BICAN) ist die nächste Stufe in den Bemühungen der NIH BRAIN Initiative, die Zellen und Zellfunktionen des Gehirns von Säugetieren zu verstehen. BICAN ist ein transformatives Projekt, das zusammen mit zwei anderen Großprojekten – der BRAIN Initiative Connectivity Across Scales und dem Armamentarium for Precision Brain Cell Access – darauf abzielt, die neurowissenschaftliche Forschung zu revolutionieren, indem es grundlegende Prinzipien beleuchtet, die die Schaltkreise des Verhaltens bestimmen, und neue Ansätze liefert zur Behandlung menschlicher Gehirnstörungen.
Referenz: „Ein hochauflösender transkriptomischer und räumlicher Atlas der Zelltypen im gesamten Maushirn“ von Zizhen Yao, Cindy TJ van Velthoven, Michael Kunst, Meng Zhang, Delissa McMillen, Changkyu Lee, Won Jung, Jeff Goldy, Aliya Abdelhak, Matthew Aitken, Katherine Baker, Pamela Baker, Eliza Barkan, Darren Bertagnolli, Ashwin Bhandiwad, Cameron Bielstein, Prajal Bishwakarma, Jazmin Campos, Daniel Carey, Tamara Casper, Anish Bhaswanth Chakka, Rushil Chakrabarty, Sakshi Chavan, Min Chen, Michael Clark, Jennie Close, Kirsten Crichton, Scott Daniel, Peter DiValentin, Tim Dolbeare, Lauren Ellingwood, Elysha Fiabane, Timothy Fliss, James Gee, James Gerstenberger, Alexandra Glandon, Jessica Gloe, Joshua Gould, James Gray, Nathan Guilford, Junitta Guzman, Daniel Hirschstein, Windy Ho, Marcus Hooper, Mike Huang, Madie Hupp, Kelly Jin, Matthew Kroll, Kanan Lathia, Arielle Leon, Su Li, Brian Long, Zach Madigan, Jessica Malloy, Jocelin Malone, Zoe Maltzer, Naomi Martin, Rachel McCue, Ryan McGinty , Nicholas Mei, Jose Melchor, Emma Meyerdierks, Tyler Mollenkopf, Skyler Moonsman, Thuc Nghi Nguyen, Sven Otto, Trangthanh Pham, Christine Rimorin, Augustin Ruiz, Raymond Sanchez, Lane Sawyer, Nadiya Shapovalova, Noah Shepard, Cliff Slaughterbeck, Josef Sulc, Michael Tieu, Amy Torkelson, Herman Tung, Nasmil Valera Cuevas, Shane Vance, Katherine Wadhwani, Katelyn Ward, Boaz Levi, Colin Farrell, Rob Young, Brian Staats, Ming-Qiang Michael Wang, Carol L. Thompson, Shoaib Mufti, Chelsea M . Pagan, Lauren Kruse, Nick Dee, Susan M. Sunkin, Luke Esposito, Michael J. Hawrylycz, Jack Waters, Lydia Ng, Kimberly Smith, Bosiljka Tasic, Xiaowei Zhuang und Hongkui Zeng, 13. Dezember 2023, Natur.
DOI: 10.1038/s41586-023-06812-z

