Novavax beantragt ENDLICH die FDA-Zulassung für die lang erwartete Covid-Impfung, von der angenommen wird, dass sie die bisher effektivste ist
- Novavax hat der FDA endlich Daten für seinen lang erwarteten COVID-19-Impfstoff vorgelegt, um die behördliche Genehmigung zu erhalten
- Der Shot mit zwei Dosen wurde für seine Sicherheit und Wirksamkeit gelobt, obwohl er wiederholt mit Verzögerungen konfrontiert war
- Klinische Studien zeigen, dass der Schuss bei der Verhinderung einer symptomatischen Covid-Infektion zu 90 % wirksam ist, aber die Daten wurden vor dem Aufkommen der Omicron-Variante gesammelt
- Falls zugelassen, wird die Novavax-Impfung die erste proteinbasierte Covid-Impfung sein, die in den USA verwendet wird
Ein weiterer Impfstoff könnte bald zu Amerikas Arsenal im Kampf gegen COVID-19 hinzugefügt werden, da Novavax bekannt gab, dass es Daten für seinen Covid-Impfstoff an die Food and Drug Administration (FDA) übermittelt hat.
Der lang erwartete Schuss sollte 2021 eingeführt werden, war jedoch im vergangenen Jahr wiederholt mit Verzögerungen konfrontiert, die das Unternehmen auf Lieferprobleme zurückführt.
Jetzt hat das Unternehmen endlich Daten zur Vorlage bei den Aufsichtsbehörden vorbereitet, die zeigen, dass sein Zwei-Schuss-Impfstoff zu 90 Prozent gegen das Virus wirksam ist – obwohl die Daten vor der Entdeckung der impfstoffresistenten Omicron-Variante Ende letzten Jahres gesammelt wurden.
Die Impfung wurde nach ersten Versuchen als die bisher sicherste und wirksamste gepriesen, und es handelt sich um einen „proteinbasierten“ Impfstoff, der das Immunsystem einer Person in inaktive Viruszellen einführt – ähnlich wie bei der Grippeimpfung und vielen anderen gängigen Impfstoffen – um dies zu tun eine Antwort montieren.
Novavax hat der FDA Daten für seinen Zwei-Schuss-COVID-19-Impfstoff vorgelegt, um die Notfallzulassung der FDA für die Verwendung in den USA zu erhalten (Aktenfoto).
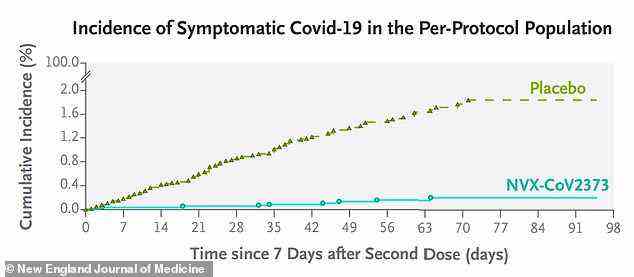
In klinischen Studien zeigte der Impfstoff, dass er zu 90 % wirksam bei der Vorbeugung einer symptomatischen Covid-Infektion war. Versuche wurden jedoch vor dem Auftauchen der Omicron-Variante durchgeführt
‘Wir sind sehr stolz auf die Arbeit unserer Teams und freuen uns auf die Überprüfung unserer durch die FDA [emergency use authorization] Anfrage”, sagte Stanley Erck, CEO von Novavax, in einer Erklärung.
„Wir glauben, dass unser Impfstoff eine differenzierte Option bietet, die auf einer gut verstandenen proteinbasierten Impfstoffplattform aufbaut, die eine Alternative zum Portfolio verfügbarer Impfstoffe sein kann, um zur Bekämpfung der COVID-19-Pandemie beizutragen.“
Das Unternehmen veröffentlichte die Ergebnisse der Phase-3-Studie im New England Journal of Medicine.
Die Studien umfassten 30.000 Teilnehmer in den USA und Mexiko und eine zweite Studie mit 15.000 Teilnehmern in Großbritannien.
Beide Studien wurden Ende 2020 und Anfang 2021 durchgeführt, was bedeutet, dass sie vor dem Aufstieg der Omicron-Variante stattfanden. Das Unternehmen machte weder in der Studie noch in der entsprechenden Stellungnahme Angaben zur Wechselwirkung der Impfung mit Omicron.
DailyMail.com wandte sich an Novavax, um Informationen darüber zu erhalten, ob der Schuss gegen den neuen Stamm wirksam ist, und erhielt nicht sofort eine Antwort.
Die erste Studie in Nordamerika ergab, dass der Impfstoff eine 90,4-prozentige Wirksamkeit bei der Verhinderung einer symptomatischen Covid-Infektion hatte. Die britische Studie ergab, dass der Stich eine Wirksamkeit von 89,7 Prozent hatte.
Die Wirksamkeit gegen Omicron kann jedoch der Schlüssel dazu sein, ob der Stich die Zulassung erhält, da die FDA gezeigt hat, dass sie bereit ist, die Zulassung von Behandlungen zu entziehen, die gegen andere Stämme, aber nicht gegen diesen, wirksam sind.
Novavax weist darauf hin, dass die häufigsten Nebenwirkungen der Injektion in Studien Kopfschmerzen, Übelkeit oder Erbrechen, Myalgie, Arthralgie, Empfindlichkeit/Schmerzen an der Injektionsstelle, Müdigkeit und Unwohlsein waren.
Der Novavax-Impfstoff wurde aufgrund seiner hohen Wirksamkeit und seines eher standardisierten Impfansatzes mit Spannung erwartet.
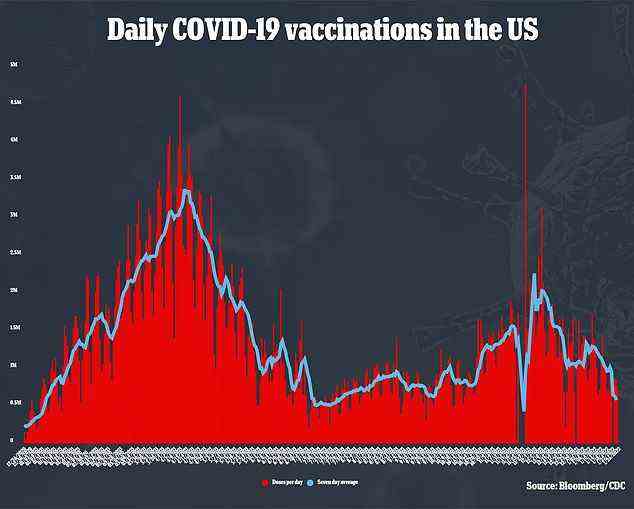
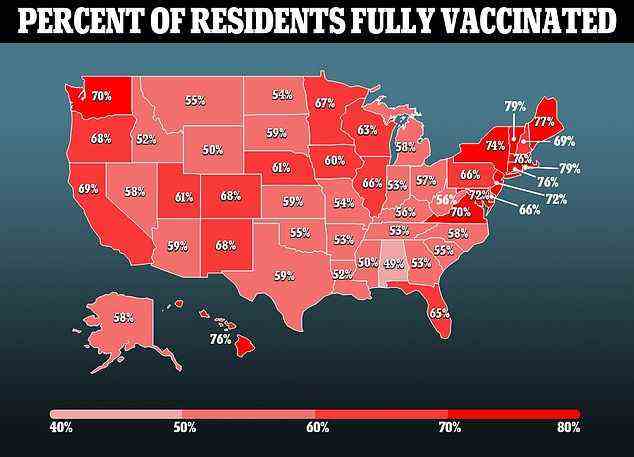
Einige, die Angst vor der mRNA-Technologie in den Impfstoffen von Pfizer-BioNTech und Moderna haben, sind möglicherweise bereit, sie zu nehmen.
„In den USA wird der Hauptmarkt meiner Meinung nach im Jahr 2022 darin bestehen, einen Impfstoff, unser normales Zwei-Dosen-Regime, an viele Menschen zu liefern, die gezögert haben, andere Impfstoffe zu bekommen“, sagte Erck im November gegenüber CNN.
Der Impfstoff kann auch bei Temperaturen von bis zu 45 ° F gelagert werden, was den Transport der Impfung erheblich erleichtert – insbesondere in Entwicklungsländern.
Das Unternehmen war in den letzten Monaten mit Produktionsproblemen konfrontiert, die zu Verzögerungen führten.
Wenn der Stich die FDA-Zulassung erhält, ist es der vierte in den USA und der dritte Zwei-Schuss-Stoß.
Der Pfizer-BioNTech-Impfstoff und jetzt der Moderna-Impfstoff, der am Montag zugelassen wurde, sind die einzigen beiden Impfungen, die von der FDA vollständig zugelassen wurden.
Das Unternehmen hat auch an einer neuen Grippeimpfung gearbeitet, die Teil des Covid-Impfschemas sein kann.