Tag: ModernaBooster
Wenn die Omikronen ansteigen, verkürzt CDC die Wartezeit für die Moderna-Booster auf 5 Monate
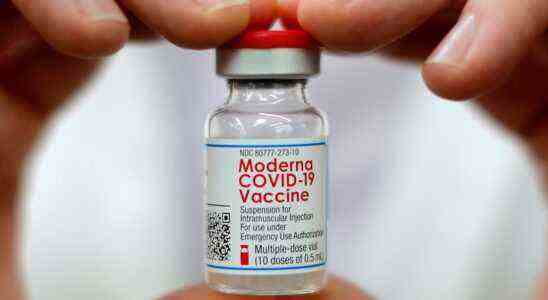
Da immer mehr Amerikaner Auffrischungsdosen von COVID-19-Impfstoffen inmitten eines Anstiegs der Omicron-Variante erhalten, sagten die Centers for Disease Control and Prevention (CDC), dass sie ihre Moderna-Booster-Empfehlung ändern würden.
„CDC passt unsere Empfehlung an, wann Menschen eine Auffrischimpfung erhalten können, und verkürzt das Intervall von sechs Monaten auf fünf Monate“, schrieb die Agentur am Freitag.
MODERNA CEO DRUCKT AUF ZWEITEN COVID-19 BOOSTER SHOT, ABER DIE ÄRZTE SIND NOCH NICHT ÜBERZEUGT, DASS ES NOTWENDIG IST
Die Empfehlung, so erklärte die CDC, bedeutet,
Moderna-Booster bietet in „beruhigender“ Studie eine signifikante Antikörperreaktion auf Omicron
Eine DRITTE Dosis des Moderna-Impfstoffs bot in einer “beruhigenden” Studie eine signifikante Antikörperantwort im Immunsystem.
source site
Coronavirus-Impfstoffe: FDA genehmigt Pfizer- und Moderna-Booster für Erwachsene
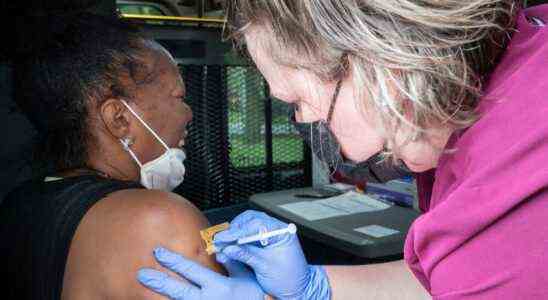
Ein Patient erhält am 29. September 2021 in einer Pfizer-BioNTech-Impfklinik in Southfield, Michigan, einen Coronavirus-Impfstoff-Booster. (Emily Elconin/Reuters)
Die Food and Drug Administration hat die Auffrischungsimpfung von Pfizer und Moderna COVID für Amerikaner ab 18 Jahren genehmigt.
Am Donnerstag erteilte die Behörde eine Notfallgenehmigung für eine dritte Dosis der Impfstoffe Pfizer-BioNTech und Moderna zur Stärkung der Immunantwort bei Personen, die die ersten beiden erhielten, deren Wirksamkeit im Laufe der Zeit nachweislich nachgelassen hat. Die Delta-Variante des Virus, ein hochgradig übertragbarer Stamm,
FDA-Panel grünes Licht für Moderna-Booster für Personen mit hohem Risiko
neues Video geladen: FDA-Panel grünes Licht für Moderna-Booster für Personen mit hohem Risiko
transkript
transkript
FDA-Panel grünes Licht für Moderna-Booster für Personen mit hohem Risiko
Ein Beratungsgremium der Food and Drug Administration empfahl eine halbe Dosis als dritte Injektion für Personen ab 65 Jahren sowie jüngere Erwachsene mit einem hohen Risiko aufgrund ihrer Erkrankungen oder Berufe.
-
„Unterstützen die verfügbaren Daten die Sicherheit und Wirksamkeit des Moderna-Covid-19-Impfstoffs zur Anwendung unter EUA als Auffrischungsdosis, 50 Mikrogramm mRNA-1273, mindestens sechs Monate nach