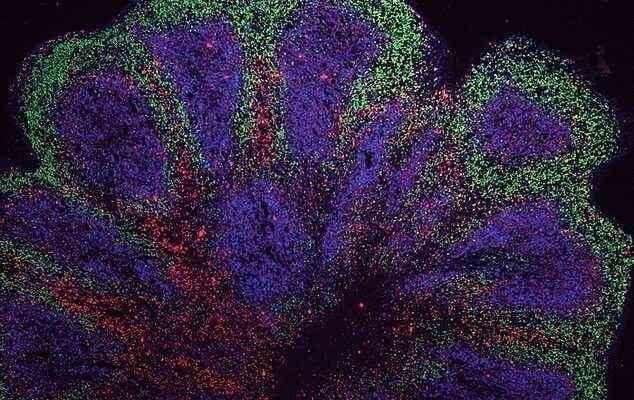
Mini-Gehirne wurden im Labor aus Zellen von Demenz- und Motoneuronpatienten gezüchtet, was die Tür für neue Behandlungen öffnet.
Die Möglichkeit, kleine organähnliche Modelle des Gehirns zu züchten, ermöglichte es Forschern der University of Cambridge, zu verstehen, was in den frühesten Stadien einer Form der Motoneuron-Erkrankung, die als amyotrophe Lateralsklerose bekannt ist, passiert.
Dieser Zustand überschneidet sich oft mit Demenz und tritt tendenziell bei jüngeren Erwachsenen im Alter von 40 bis 45 Jahren auf.
Die Mini-Gehirne helfen Wissenschaftlern zu sehen, wie sich die Erkrankung entwickelt, lange bevor irgendwelche Symptome auftreten, und wiederum nach möglichen Medikamenten zu suchen.
Diese Erkrankungen verursachen verheerende Symptome einer Muskelschwäche mit Veränderungen des Gedächtnisses, des Verhaltens und der Persönlichkeit, die gelindert werden können, wenn sie früh genug erkannt werden.
In Zukunft hoffen die Forscher, dass aus den Hautzellen eines Menschen individuelle Mini-Gehirne hergestellt werden könnten, um personalisierte Medikamente zur Behandlung ihrer spezifischen Symptome zu entwickeln und zu testen.
Mini-Gehirne wurden im Labor aus Zellen von Demenz- und Motoneuronpatienten gezüchtet, was laut Forschern die Tür für neue Behandlungen öffnet
Ein Medikament, das an künstlichen Gehirnen getestet wurde, zerstörte toxische Proteine, die sich in Klumpen ansammeln, sagen Wissenschaftler der Universität Cambridge.
Studienleiter Dr. Andras Lakatos sagte: „Neurodegenerative Erkrankungen sind sehr komplexe Erkrankungen, die viele verschiedene Zelltypen betreffen können und wie diese Zellen im Verlauf der Erkrankung zu verschiedenen Zeiten interagieren.
„Um dieser Komplexität nahe zu kommen, brauchen wir Modelle, die langlebiger sind und die Zusammensetzung der menschlichen Gehirnzellpopulationen, in denen typischerweise Störungen auftreten, nachbilden, und genau das bietet unser Ansatz.
“Wir können nicht nur sehen, was in einem frühen Stadium der Krankheit passieren kann – lange bevor ein Patient irgendwelche Symptome verspürt -, sondern wir können auch sehen, wie sich die Störungen im Laufe der Zeit in jeder Zelle verändern.”
Die Modelle wurden fast ein Jahr lang kultiviert und ermöglichten die Analyse von Demenzerkrankungen über einen langen Zeitraum.
Sie stammten von Patienten mit FTD (frontotemporale Demenz) und ALS (amyotrophe Lateralsklerose) – einer häufigen Form der Motoneuronerkrankung.
Die Erkrankungen verursachen Muskelschwäche und Gedächtnis-, Verhaltens- und Persönlichkeitsprobleme – und können Menschen zwischen 30 und 40 betreffen.
Die Mini-Gehirne oder „Organoide“ zeigen, was passiert, lange bevor Symptome auftreten, und können mögliche Therapien durchsuchen.
Hirngewebe, das zuvor im Labor hergestellt wurde, hat nur kurze Zeit gehalten, was den Spielraum für Experimente einschränkt, aber dieses Experiment überlebte 340 Tage.
Während dieser Zeit beherbergte es die häufigste genetische Mutation bei FTD und ALS.
Anstelle von Zellkugeln wurden die 3D-Kulturen in Scheiben geschnitten, um sicherzustellen, dass sie den notwendigen Brennstoff erhielten.
“Wenn die Zellen in größeren Kugeln gruppiert sind, erhalten diese Zellen im Kern möglicherweise nicht genügend Nahrung”, sagte Erstautorin Dr. Kornelia Szebenyi.
“Dies könnte erklären, warum frühere Versuche, Organoide langfristig aus Patientenzellen zu züchten, schwierig waren”, erklärten die Forscher.
Es zeigte Veränderungen in einem sehr frühen Stadium, einschließlich Stress und DNA-Schäden, die Proteine schädigen.
Gehirn- und Nervenzellen, die Astroglia genannt werden, waren betroffen und orchestrieren Muskelbewegungen und geistige Fähigkeiten.
Dr. Lakatos sagte: „Obwohl diese anfänglichen Störungen subtil waren, waren wir überrascht, wie früh Veränderungen in unserem menschlichen Modell von ALS/FTD auftraten.
„Diese und andere neuere Studien deuten darauf hin, dass der Schaden beginnen könnte, sobald wir geboren werden.
“Wir werden mehr Forschung brauchen, um zu verstehen, ob dies tatsächlich der Fall ist oder ob dieser Prozess bei Organoiden durch die künstlichen Bedingungen in der Schale vorangetrieben wird.”
Im Allgemeinen werden Organoide, die oft als „Miniorgane“ bezeichnet werden, zunehmend verwendet, um menschliche Biologie und Krankheiten zu modellieren.
Allein an der University of Cambridge verwenden Forscher sie unter anderem, um geschädigte Lebern zu reparieren, die SARS-CoV-2-Infektion der Lunge zu untersuchen und die frühen Stadien der Schwangerschaft zu modellieren.
Typischerweise entnehmen Forscher Zellen der Haut eines Patienten und reprogrammieren die Zellen zurück in ihr Stammzellstadium – ein sehr frühes Entwicklungsstadium, in dem sie das Potenzial haben, sich zu den meisten Zelltypen zu entwickeln.
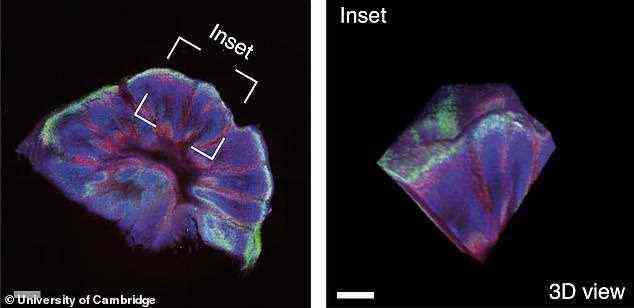
Ein Medikament, das an künstlichen Gehirnen getestet wurde, zerstörte toxische Proteine, die sich in Klumpen ansammeln, sagen Wissenschaftler der Universität Cambridge
Da viele Krankheiten zum Teil durch Defekte in unserer DNA verursacht werden, können Forscher mit dieser Technik sehen, wie zelluläre Veränderungen – oft im Zusammenhang mit diesen genetischen Mutationen – zu Krankheiten führen.
Organoide haben einen Vorteil gegenüber Tiermodellen, die oft nicht die gleichen Veränderungen des Gehirns wie beim Menschen zeigen.
Die Forscher entdeckten, dass ein bestimmtes Medikament die Ansammlung von Rogue-Proteinen bekämpft, die bei FTD und ALS auftreten.
Sie reduzierten den Zellstress und den Verlust von Nervenzellen – und blockierten damit eine der Ursachen der Erkrankungen.
Ähnliche, für den Menschen zugelassene, besser geeignete Medikamente werden derzeit in klinischen Studien für neurodegenerative Erkrankungen getestet.
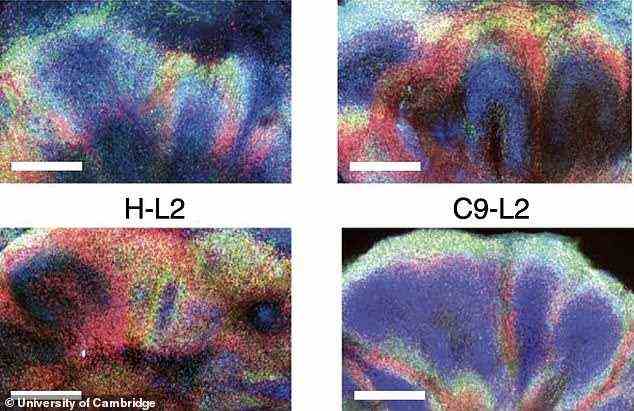
Co-Senior-Autor Dr. Gabriel Balmus vom UK Dementia Research Institute in Cambridge sagte: “Indem wir einige der Mechanismen modellieren, die zu DNA-Schäden in Nervenzellen führen, und zeigen, wie diese zu verschiedenen Zelldysfunktionen führen können, können wir möglicherweise auch in der Lage sein.” um weitere potenzielle Wirkstoffziele zu identifizieren’
Co-Senior-Autor Dr. Gabriel Balmus vom UK Dementia Research Institute in Cambridge sagte: “Indem wir einige der Mechanismen modellieren, die zu DNA-Schäden in Nervenzellen führen und zeigen, wie diese zu verschiedenen Zelldysfunktionen führen können, können wir möglicherweise auch in der Lage sein.” um weitere potenzielle Wirkstoffziele zu identifizieren.’
Das Gehirn von Patienten kann erst nach dem Tod untersucht werden. Die Organoide haben einen Vorteil gegenüber Tiermodellen, die keine ähnlichen Veränderungen zeigen.
Sie ähneln Teilen der menschlichen Großhirnrinde in Bezug auf embryonale und fetale Entwicklung, Struktur und Zellen.
Dies ist die äußere Oberfläche des Gehirns, die Bewusstsein, Denken, Emotionen, Argumentation, Sprache und Gedächtnis steuert.
Dr. Lakatos fügte hinzu: “Wir haben derzeit keine sehr wirksamen Optionen zur Behandlung von ALS/FTD, und obwohl nach unserer Entdeckung noch viel zu tun ist, gibt es zumindest Hoffnung, dass es mit der Zeit möglich sein könnte, dies zu verhindern oder zu verlangsamen.” den Krankheitsprozess.
“Es könnte in Zukunft auch möglich sein, einem Patienten Hautzellen zu entnehmen, sie so umzuprogrammieren, dass ihr ‘Mini-Gehirn’ wächst, und zu testen, welche einzigartige Kombination von Medikamenten am besten zu ihrer Krankheit passt.”
Die Studie wurde in der Zeitschrift Nature Neuroscience veröffentlicht.