Die Direktorin der Centers for Disease Control and Prevention (CDC) hat ihre Entscheidung verteidigt, das Beratungsgremium ihrer eigenen Agentur aufzuheben und zu empfehlen, dass Menschen, die aufgrund ihrer Arbeit an COVID-19 gefährdet sind, Auffrischimpfstoffe erhalten.
Am Donnerstagnachmittag sagte der Beratende Ausschuss für Immunisierungspraktiken (ACIP), dass die dritte Dosis nur für Amerikaner ab 65 Jahren und solche mit Grunderkrankungen nach sechs Monaten gelten sollte.
Die Mitglieder sagten jedoch, es gebe nicht genügend Daten, die darauf hindeuten, dass diejenigen, die in institutionellen Umgebungen leben, die ihr Expositionsrisiko erhöhen, wie Gefängnissen oder Obdachlosenheimen, sowie Gesundheitspersonal, Lehrer und Angestellte von Lebensmittelgeschäften einem erhöhten Risiko ausgesetzt sind.
Aber Dr. Rochelle Walensky war anderer Meinung und brach mit dem Ausschuss, sagte jedoch, sie habe sich ihre Bedenken angehört, bevor sie ihre Entscheidung traf.
„Ich habe einen Beratungsausschuss nicht außer Kraft gesetzt … Dies war eine wissenschaftliche Enge“, sagte sie während einer Pressekonferenz der Coronavirus-Task Force des Weißen Hauses am Freitag.
»In dieser Situation war es mein Anruf. Wenn ich im Raum gewesen wäre, hätte ich mit “Ja” gestimmt.’
CDC-Direktorin Dr. Rochelle Walensky verteidigte am Freitag (oben) ihre Entscheidung, das Beratungsgremium ihrer eigenen Agentur aufzuheben und Booster für Personen mit hohem Risiko aufgrund ihrer Arbeit zu empfehlen, und sagte, dass es ihre “Entscheidung” sei, weil es eine knappe Abstimmung war.
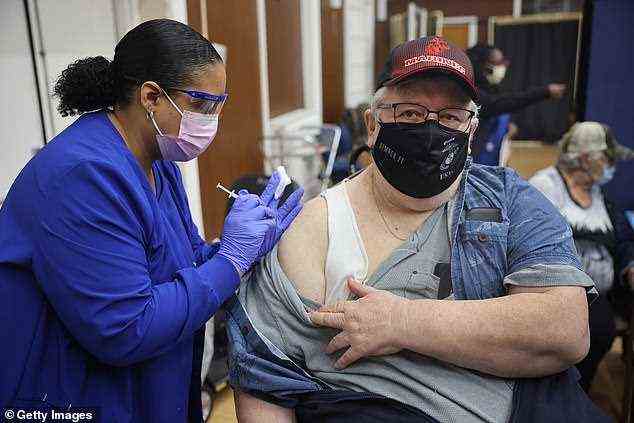
Booster-Dosen wurden auch für Personen ab 65 Jahren und alle Amerikaner mit Grunderkrankungen zugelassen. Im Bild: Shana Alesi verabreicht dem Marine Corps-Veteran Bill Fatz im Edward Hines Jr VA Hospital in Hines, Illinois, 24. September einen COVID-19-Booster
Am Donnerstagnachmittag stimmte ACIP einstimmig dafür, Menschen im Alter von 65 Jahren und älter und Bewohnern von Langzeitpflegeeinrichtungen sowie 13-2 für Amerikaner zwischen 50 und 64 Jahren mit Vorerkrankungen die Spritze zu geben.
Booster wurden auch für Personen im Alter von 18 bis 49 Jahren mit Vorerkrankungen empfohlen, aber die Abstimmung war viel enger, als die Empfehlung mit 9-6 bestanden wurde.
Der Ausschuss stimmte jedoch gegen die empfohlene Verwendung für Personen, die aufgrund eines „beruflichen oder institutionellen Umfelds“ gefährdet sind, und behauptete, es lägen nicht genügend Daten vor, um eine solche Empfehlung auszusprechen.
Bis die FDA ihre Entscheidung bekannt gab, konnte ACIP keine dritte Dosis empfehlen, ein notwendiger Schritt, bevor Apotheker oder Kliniker Patienten immunisieren können.
Obwohl die CDC nicht verpflichtet ist, den Empfehlungen der Beratungsgruppe zu folgen, verstößt die Agentur in der Regel nicht gegen die Anweisungen von ACIP.
Es war also ein überraschender Schritt am späten Donnerstagabend, als Walesnky das Beratungsgremium ihrer eigenen Agentur am späten Donnerstagabend in einem seltenen Schritt überstimmte und eine Empfehlung für COVID-19-Impfstoff-Booster für Menschen hinzufügte, die aufgrund ihrer Arbeit gefährdet waren.
Sie, die dem Gesundheitspersonal und anderen Auftrieb gibt würde “den öffentlichen Gesundheitsbedürfnissen des Landes am besten dienen”.
“In einer Pandemie müssen wir selbst bei Unsicherheit Maßnahmen ergreifen, von denen wir erwarten, dass sie den größten Nutzen bringen”, sagte Walensky in einer Erklärung.
Im vergangenen Monat wurden Booster für immungeschwächte Amerikaner zugelassen, die entweder den Pfizer- oder Moderna-Impfstoff erhalten hatten, nachdem Daten zeigten, dass sie nach zwei Dosen weniger wahrscheinlich hohe Antikörperspiegel entwickeln.
Laut Daten der CDC haben bis Freitag mindestens 2,37 Millionen Menschen in den USA Auffrischungsdosen erhalten.
Das Weiße Haus kündigte im vergangenen Monat auch an, dass ab dem 20. September Booster-Impfungen für alle Amerikaner verfügbar sein würden – ein Datum, das gekommen und gegangen ist – aufgrund von Daten, die auf eine nachlassende Wirksamkeit der ersten Schüsse hindeuten.
Zu dieser Zeit sagte Pfizer, dass seine frühen Daten darauf hindeuteten, dass Menschen, die zwischen sechs und 12 Monaten nach ihrer letzten Dosis Auffrischungsdosen erhielten, ein hohes Maß an Schutz hatten.
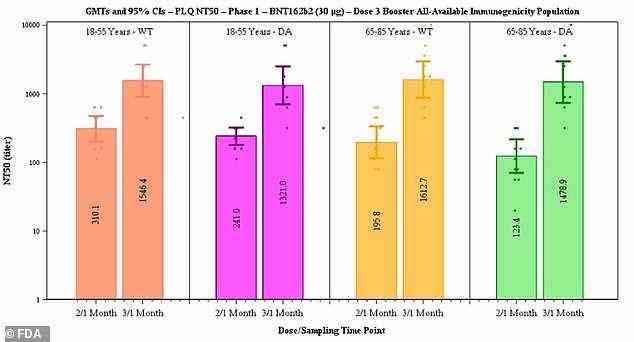
Pfizer sagte, dass die Daten darauf hindeuten, dass die Wirksamkeit von zwei Dosen nach sechs Monaten von 96,2 % auf 83,7 % sinkt, aber dass eine dritte Dosis die Antikörperspiegel erhöht (oben).
Das Unternehmen beantragte Ende August eine Notfallgenehmigung für Auffrischungsdosen und übermittelte Daten an die FDA, die letzte Woche veröffentlicht wurden.
Die Dokumente legen nahe, dass der Schutz durch zwei Dosen des Pfizer-Impfstoffs von 96,2 Prozent sieben Tage nach der zweiten Dosis auf 90,1 Prozent zwei Monate später auf 83,7 Prozent bis zu sechs Monate später abnimmt.
Darüber hinaus zitierten sie Daten aus Israel, die zeigen, dass Personen, die im Januar 2021 vollständig geimpft wurden, ein 2,26-fach erhöhtes Risiko für Durchbruchsinfektionen hatten im Vergleich zu Personen, die im April 2021 vollständig geimpft wurden.
Eine andere israelische Studie, die in den Dokumenten diskutiert wird, zeigte, dass die Wirksamkeit gegen Infektionen 39 Prozent und gegen symptomatische Erkrankungen 40 Prozent vom 20. Juni 2021 bis 17. Juli 2021 betrug, als die Delta-Variante der dominierende Stamm war.
Im Vergleich dazu lagen diese Raten zwischen Januar und April bei 95 Prozent oder höher.
Das Team veröffentlichte auch Daten aus einer klinischen Studie mit 23 Teilnehmer, die letztes Jahr an den frühen Studien von Pfizer teilgenommen haben.
Jeder hatte zwei Dosen des Impfstoffs erhalten und erhielt mindestens sechs Monate später eine Auffrischungsdosis.
Von den Teilnehmern waren 11 in der Die Gruppe der jüngeren Erwachsenen im Alter von 18 bis 55 und 12 Jahren war 65 bis 85 Jahre alt.
Nach der dritten Dosis stiegen die neutralisierenden Antikörper gegen den ursprünglichen Virusstamm in der Altersgruppe der 18- bis 55-Jährigen um das Fünffache und in der Altersgruppe der 65- bis 85-Jährigen um das Siebenfache.
Gegen die Delta-Variante stiegen die Antikörperspiegel nach einer Auffrischimpfung in der Gruppe der jüngeren Erwachsenen um das Fünffache und in der Gruppe der älteren Erwachsenen um das Zwölffache.
Aber viele Wissenschaftler, darunter hochrangige Beamte der FDA, waren mit Auffrischungsspritzen nicht einverstanden und argumentierten, dass die Impfstoffe immer noch hochwirksam sind, um schwere Krankheiten und Todesfälle zu verhindern.
FDA-Beamte äußerten sich auch besorgt über den Mangel an Daten zu den potenziellen Nebenwirkungen einer dritten Dosis, insbesondere bei jüngeren Erwachsenen, bei denen ein Risiko für Herzentzündungen besteht.
In einem separaten Briefing-Dokument, das ebenfalls letzte Woche veröffentlicht wurde, schrieben FDA-Wissenschaftler mit einem skeptischen Ton über die Notwendigkeit von Auffrischungsspritzen.
“Insgesamt weisen die Daten darauf hin, dass derzeit in den USA lizenzierte oder zugelassene COVID-19-Impfstoffe in den Vereinigten Staaten immer noch Schutz vor schwerer COVID-19-Erkrankung und dem Tod bieten”, schrieben die Wissenschaftler.
Sie fügten hinzu, dass Studien zu Booster-Dosen widersprüchliche Ergebnisse gezeigt haben und dass “bekannte und unbekannte Verzerrungen, die ihre Zuverlässigkeit beeinträchtigen können.”

